නූතන අවර්තිතා වගුව
මේ වන විට මූලද්රව්ය 115 කට වඩා වැඩි සංඛ්යාවක් සොයාගෙන ඇත. ඒවායේ ගුණ වෙන් වෙන් ව අධ්යයනය කිරීම ඉතා අපහසු කටයුත්තකි. මූලද්රව්යවල සහ ඒවායේ සංයෝගවල තොරතුරු ලෝකයේ විද්යාඥයින් විසින් නොකඩවා රැස් කරනු ලැබේ. මේ තොරතුරු සම්භාරය කෙතරම් විශාල ද විවිධ ද යත් සියලු කරුණු මතක තබා ගැනීම කිසිවෙකුටත් කළ නොහැක්කකි. මේ නිසා විවිධ විද්යාඥයින් විසින් මූලද්රව්ය විවිධ ක්රම අනුව වර්ග කිරීමට උත්සාහ දරා ඇත. එම උත්සාහයේ අග්රගණ්ය ප්රතිඵලයකි ආවර්තිතා වර්ගීකරණය. මූලද්රව්ය වර්ගීකරණය සඳහා ආවර්තිතා වගුවක් මුලින් ම ඉදිරිපත් කරන ලද්දේ රුසියානු ජාතික විද්යාඥයෙක් වන ද්මිත්රී මෙන්ඩලීෆ් විසිනි.
■ නූතන ආවර්තිතා නියමය
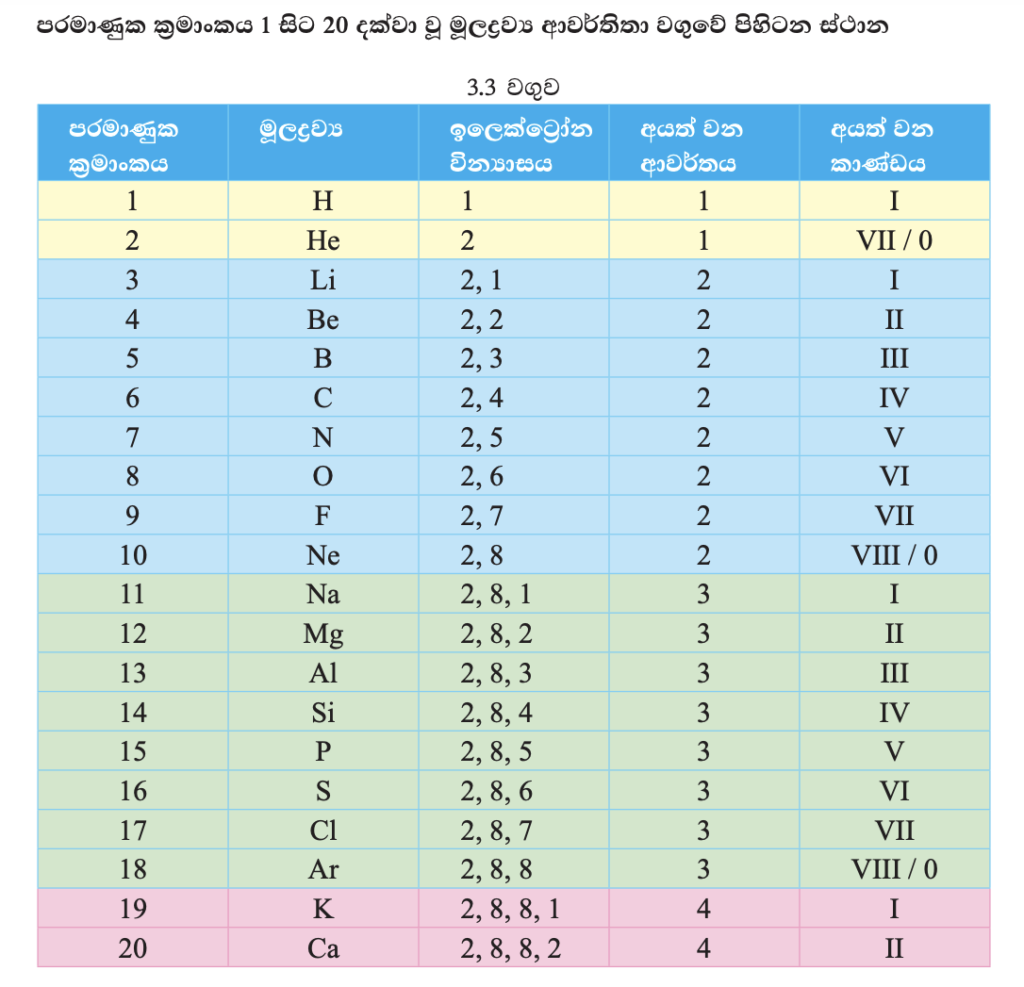
නූතන ආවර්තිතා වගුව (3.3 රූපය) පදනම් වී ඇත්තේ පරමාණුක ක්රමාංකය හා ඉලෙක්ට්රෝන වින්යාසය මතයි. ඉන් කියැවෙන්නේ මූලද්රව්යවල ගුණ ඒවායේ පරමාණුක ක්රමාංකවල ආවර්තිතා ශ්රිතයක් බවයි. ඉන් අදහස් වනුයේ පරමාණුක ක්රමාංකය ආරෝහණය වන පිළිවෙළට මූලද්රව්ය සකස් කළ විට කිසියම් මූලද්රව්ය පරාසයකට පසුව සමාන ගුණ සහිත මූලද්රව්ය යළිත් හමුවෙන බවයි.

■ මූලද්රව්ය ආවර්තවලට බෙදීම
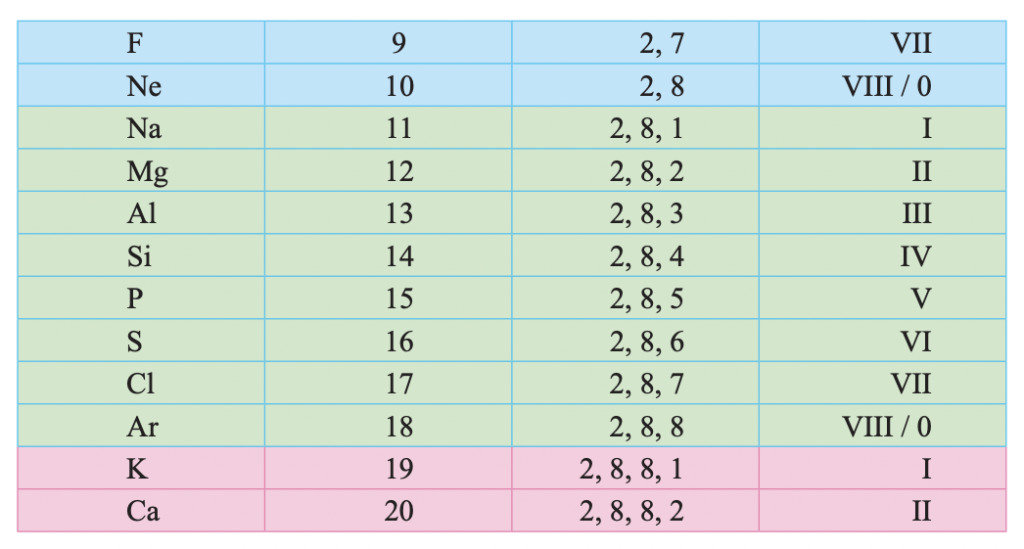
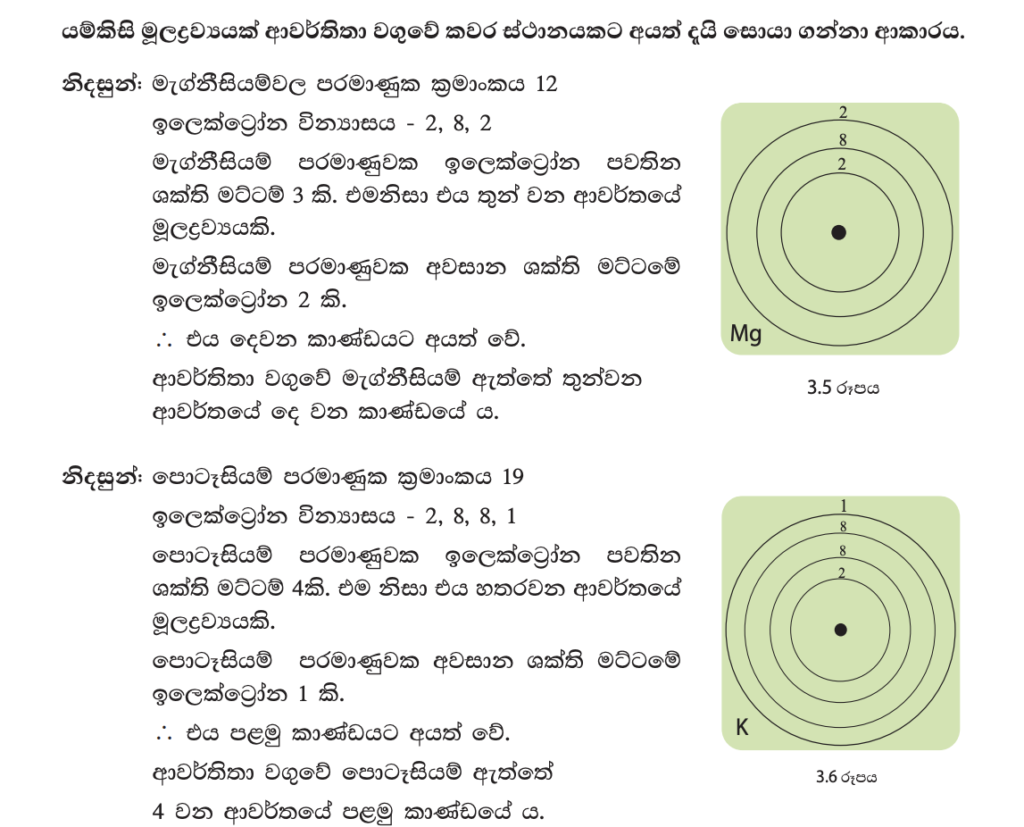
යම් මූලද්රව්යයක් අයත් වන්නේ ආවර්තිතා වගුවේ කවර ආවර්තයට ද යන්න තීරණය වන්නේ එම මූලද්රව්යයේ පරමාණුවක තිබෙන ඉලෙක්ට්රෝන ව්යාප්ත ව පවතින “ශක්ති මට්ටම්” (කවච) ගණනෙනි.

■ මූලද්රව්ය කාණ්ඩවලට බෙදීම
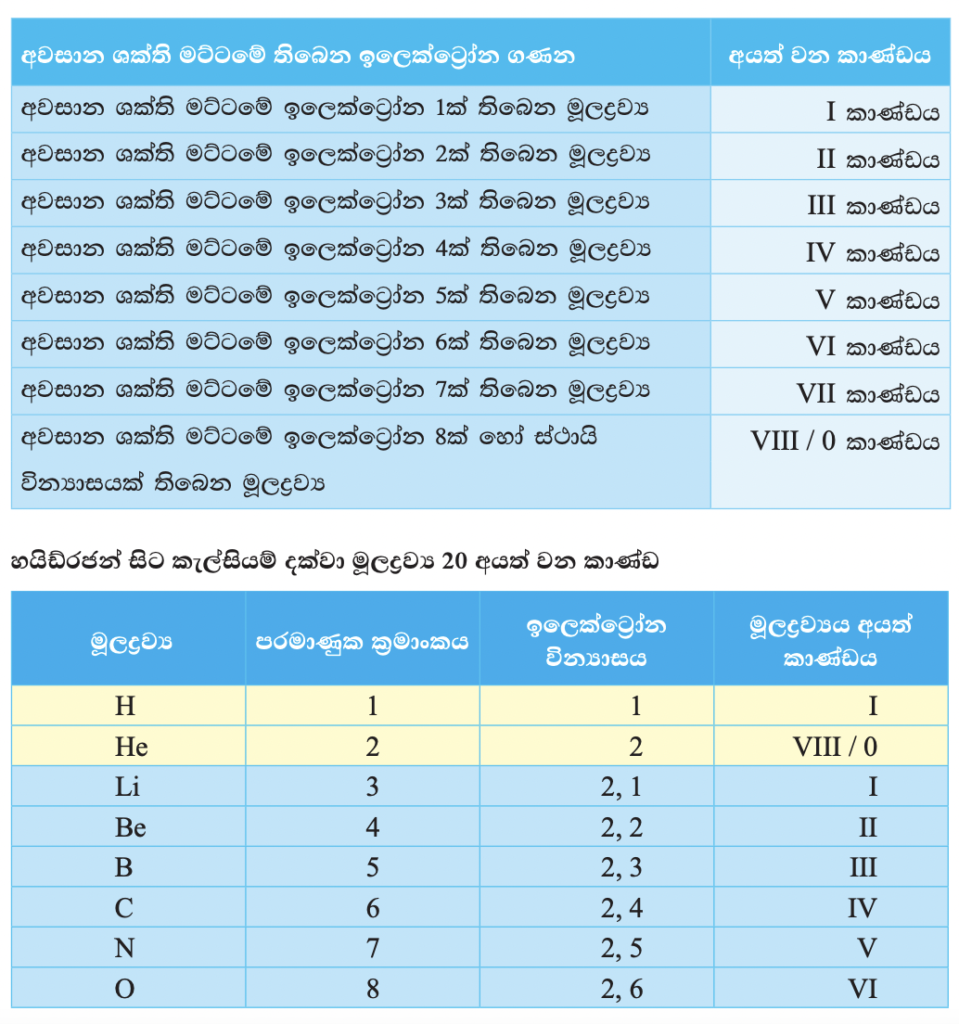
මූලද්රව්යයක ගුණ රඳා පවතින්නේ එහි අවසාන ශක්ති මට්ටමේ ඇති ඉලෙක්ට්රෝන සංඛ්යාව මතයි. මේවා සංයුජතා ඉලෙක්ට්රෝන යනුවෙන් හැඳින්වේ. මූල ද්රව්යයක ගුණ බොහෝ දුරට එහි අවසාන ශක්ති මට්ටමේ ඇති ඉලෙක්ට්රෝන ගණන මත රදා පවතී. ඉහත වගුව අනුව ලිතියම්,සෝඩියම් හා පොටෑසියම්වල අවසාන ශක්ති මට්ටමේ ඉලෙක්ට්රෝන එකක් පමණක් ඇත. එබැවින් පෙනෙන්නේ සංයුජතා ඉලෙක්ට්රෝන එකක් පමණක් ඇති ලිතියම්, සෝඩියම් හා පොටෑසියම්වල රසායනික ගුණ බොහෝ දුරට සමාන බවයි. මෙම මූලද්රව්ය තුනම ආවර්තිතා වගුවේ එකම සිරස් පේළියේ පවතී.
මෙසේ ඉහළ තිරස් පේළියේ ඇති ඕනෑ ම මූලද්රව්යයක ගතිගුණ ඊට පහළින් ඇති මූලද්රව්යයේ ගතිගුණවලට සමාන වන බව පෙනේ. යම් මූලද්රව්යයක් අයත් වන කාණ්ඩය තීරණය වන්නේ එහි අවසාන ශක්ති මට්ටමේ අඩංගු ඉලෙක්ට්රෝන ගණන අනුව ය.